1) Introduction
Alors que certains insectes prédateurs chassent « à courre » ou, au vol, d’autres adoptent une position immobile et capturent à distance leurs proies grâce à leurs pattes avant ou à leurs pièces buccales modifiées. Il en est ainsi pour les mantes, Mantis religiosa (1) ou de certaines punaises Empicoris rubrumaculatus (2) qui projettent leurs pattes antérieures ravisseuses ou des larves de libellules (3) avec leur lèvre inférieure transformée en organe préhenseur (appelé le masque).
Une attaque rapide associée à une excellente acuité visuelle assure souvent le succès de la capture du gibier convoité.

Cet article s’inspire de travaux de plusieurs chercheurs (références à la fin de ce chapitre) et met en lumière deux stratégies de prédation utilisées par toutes les espèces d’un genre de Staphylinidae, les Stenus Latreille, 1796. Ces staphylins utilisent, à l’état adulte, soit leurs mandibules, soit un « harpon » pour attraper leurs proies, souvent des collemboles.
En illustration de l'article qui suit, cliquer sur l'image ci-dessous pour accéder à une vidéo qui montre des harponnages de staphylins.
2) Le prédateur
 Un Stenus est un Coléoptère doté d’un labium extensible (lèvre inférieure complexe), qui lui permet de pratiquer une chasse d’approche ou d’affût. Ses proies se déplacent, comme lui, sur le sol ou sur les végétaux. C’est le cas de certaines espèces de collemboles qui, outre la fuite en courant, peuvent aussi sauter en utilisant leur furca (organe sauteur qui se déclenche au moindre stimulus).
Un Stenus est un Coléoptère doté d’un labium extensible (lèvre inférieure complexe), qui lui permet de pratiquer une chasse d’approche ou d’affût. Ses proies se déplacent, comme lui, sur le sol ou sur les végétaux. C’est le cas de certaines espèces de collemboles qui, outre la fuite en courant, peuvent aussi sauter en utilisant leur furca (organe sauteur qui se déclenche au moindre stimulus).
Cette fuite se fait à des vitesses sensiblement identiques chez différentes espèces de collemboles ; et donc, si le Stenus veut attraper ces collemboles, il devra, à minima, courir aussi vite.
Le labium du Stenus est capable de s’allonger à une vitesse fulgurante pour atteindre sa proie et l‘immobiliser grâce à des « coussinets » particuliers, comme nous allons le découvrir. Le labium se rétracte ensuite rapidement et la proie est saisie par les deux fines mandibules.
Dans le cadre d’une étude conduite sur la chasse pratiquée par les Stenus, des entomologistes allemands ont observé trois espèces de collemboles (les proies) et noté par ailleurs que, pour près de la moitié de leurs attaques, les Stenus utilisent leur labium extensible.
Photo ci-contre: Stenus bimaculatus Gyllenhal, 1810 © A.Wojtyra.
3) Les Proies
Les photos-montages ci-dessous illustrent les morphologies des trois espèces de collemboles qui ont servi de proies aux Stenus. En encart, détail de leurs revêtements cuticulaires qui sera déterminant dans le succès des captures.
Heteromurus nitidus (Templeton & Westwood, 1836): Entomobryomorphe qui se déplace en surface sur des sols plutôt secs, son corps est recouvert d’écailles et de quelques longues soies.

Heteromurus nitidus : photographie d’un individu en vue dorsale dans son biotope naturel © Ph.Garcelon ; en encart, photo au microscope électronique à balayage de l’abdomen montrant les écailles (© T.Bauer & M.Pfeiffer).
Podura aquatica (Linné, 1758): Poduromorphe qui affectionne les milieux humides et évolue fréquemment à la surface de l’eau. Son corps est couvert de petits tubercules avec très peu de soies courtes.
 Podura aquatica : photographie d’un individu en vue dorsale dans son biotope naturel © Ph.Garcelon ; en encart, photo au microscope électronique à balayage de l’abdomen, © T.Bauer & M.Pfeiffer, montrant les microtubercules et les quelques soies sensorielles.
Podura aquatica : photographie d’un individu en vue dorsale dans son biotope naturel © Ph.Garcelon ; en encart, photo au microscope électronique à balayage de l’abdomen, © T.Bauer & M.Pfeiffer, montrant les microtubercules et les quelques soies sensorielles.
Isotomurus palustris (Muller, 1776): Entomobryomorphe qui évolue essentiellement dans des zones humides en bordure immédiate d’étangs ou de lacs. Son corps est entièrement recouvert de soies.
 Isotomurus palustris : photographie d’un individu en vue dorsale dans son biotope naturel © Ph.Garcelon; en encart, photo au microscope électronique à balayage de l’abdomen, © T.Bauer & M.Pfeiffer, montrant les différentes soies sensorielles.
Isotomurus palustris : photographie d’un individu en vue dorsale dans son biotope naturel © Ph.Garcelon; en encart, photo au microscope électronique à balayage de l’abdomen, © T.Bauer & M.Pfeiffer, montrant les différentes soies sensorielles.
4) Découvrons ces Stenus prédateurs
La sous-famille des Steninae comprend plus de 3300 espèces réparties entre deux genres actuels1 : les Stenus Latreille, 1796 et les Dianous Leach, 1819. 24 espèces fossiles ont aussi été décrites dans ces deux genres, mais aussi dans d’autres genres comme Eocenostenus Cai, 2014 (une espèce du paléogène2 de France) et Festenus Zyla, 2017 (2 espèces du crétacé supérieur3 de Birmanie). Les Steninae sont des coléoptères appartenant à la très diversifiée famille des Staphylinidae, l’un des taxons, avec les Curculionidae (ou charançons), le plus riche en espèces du règne animal (plus de 65000 espèces connues).
Un peu plus de 3000 espèces apparaissent dans le seul genre Stenus, ce qui en fait le deuxième plus important à l’échelle animale. La grande majorité des espèces vit dans les forêts tropicales. Un peu moins de 150 espèces s’observent à travers toute la France.
Leur répartition est mondiale, à l'exception toutefois de l'Antarctique et de la Nouvelle-Zélande.
Ces staphylins, de taille petite à moyenne (± 1 à 10 mm) s’observent le plus souvent : (1) dans des habitats liés à l'humus humide ou des débris végétaux près du sol, (2) sur le sol nu, ou (3) sur des plantes fréquemment au bord de l’eau.
Les Stenus sont des espèces vagiles, poursuivant donc leurs proies sur le sol ou parmi la végétation, mais jamais en volant. Ils chassent à vue de nombreux invertébrés, tels des vers oligochètes (comme le lombric), des acariens, des araignées, des pucerons ou encore (et surtout) des collemboles. À la manière d’autres prédateurs, ils capturent leurs proies avec leurs deux mandibules en forme de faux. Ou alors, ils attrapent leurs « gibiers » à l’affût et à distance grâce à un labium « télescopique » unique, utilisé tel un harpon. Il est l'une des structures de capture de proies les plus spécialisées chez les insectes. Nous y reviendrons plus loin.
Cette sous-famille se reconnaît facilement à son habitus général très typé.
- 1 Un troisième genre australien est en attente de description.
- 2 Crétacé supérieur : Période géologique comprise entre 100,5 à 66,0 millions d'années. Elle se termine avec une extinction massive, l'extinction Crétacé-Tertiaire.
- 3 Paléogène : période géologique succédant au Crétacé qui s'étend de 66,0 à 23,03 millions d'années.
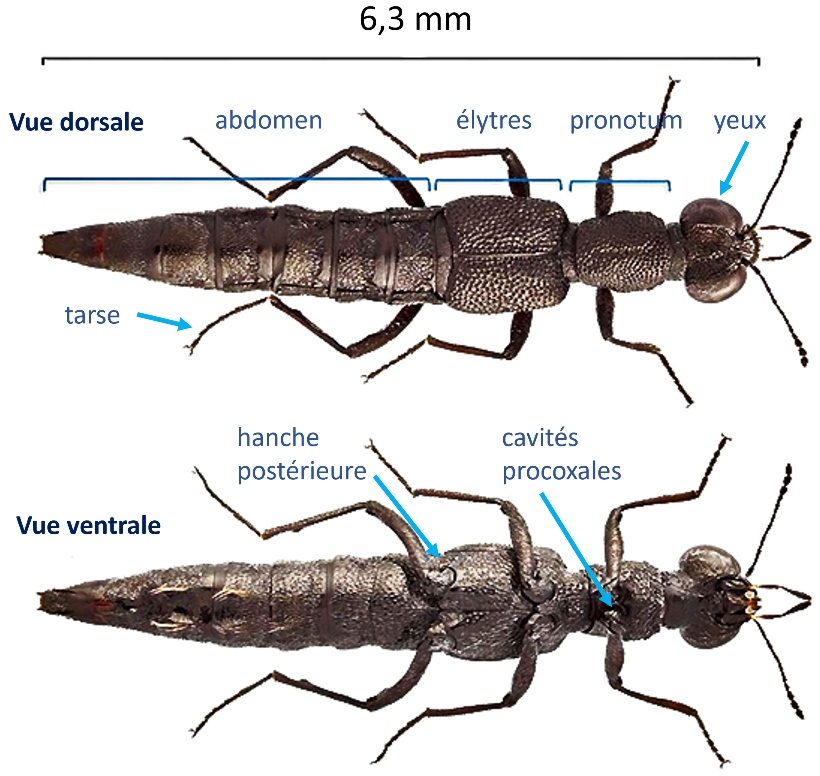 Habitus de Stenus ater -Mannerheim, 1830. Modifié à partir d’une photo de © E. Gay.
Habitus de Stenus ater -Mannerheim, 1830. Modifié à partir d’une photo de © E. Gay.
Les Steninae adultes (voir photos ci-dessus) possèdent deux gros yeux hémisphériques qui occupent presque l’entièreté des côtés de la tête, de la base des mandibules au cou. Ils sont porteurs de très nombreuses ommatidies uniformément réparties sur toute la surface oculaire, ce qui explique la très bonne acuité visuelle de ces staphylins.
Les antennes comprennent 11 segments ou antennomères (avec les deux antennomères basaux plus épais et une massue terminale plus ou moins marquée composée de 3 antennomères) ; elles prennent naissance sur le vertex entre les yeux.
Le pronotum – partie dorsale du prothorax – a une forme cylindrique sans marges latérales. Les élytres courts sont tapissés d’une ponctuation piligère dense, ils ne font pas saillie sur le métathorax et ne possèdent pas de carène latérale (épipleurale).
Les hanches antérieures sont peu développées ; de forme conique, elles se logent et s’articulent dans des cavités coxales antérieures entièrement fermées. Les hanches postérieures sont, quant à elles, nettement séparées. Tous les tarses possèdent cinq articles (pentamères).
L’abdomen est allongé et à une section cylindrique, un rebord est présent ou pas sur les tergites. L’édéage (structure génitale du mâle) est symétrique (photos ci-dessous).
 Edéage de Stenus ater. Longueur maximale : 0.7 mm- modifié d’après © E. Gay.
Edéage de Stenus ater. Longueur maximale : 0.7 mm- modifié d’après © E. Gay.
Cet organe, comprend une pièce centrale, le lobe médian, sur lequel s’articulent deux paramères. La spermathèque des femelles est sclérotisée ou pas. Les Dianous se distinguent aisément des Stenus par deux styles plus ou moins longs à l’extrémité de l’abdomen.
Revenons et détaillons ce « harpon », caractéristique des Stenus.
Alors que le labium des coléoptères Dianous est court et non spécialisé, les espèces de Stenus sont toutes caractérisées par un labium allongé et proéminent qui fonctionne tel un appareil de capture des proies à distance. Noter qu’il était déjà présent chez les espèces fossiles du genre Festenus.
Le labium peut être projeté vers une proie potentielle en quelques millisecondes et ce, par la seule pression de l'hémolymphe. Une fois touchée par les coussinets adhésifs, la proie est fixée et, après la rétraction rapide du labium (30-40 m/s), saisie par les mandibules du coléoptère. Remarquons que tous les Stenus étudiés jusqu'à présent sont aussi capables d'attraper leurs proies directement avec les mandibules sans utiliser leur labium spécialisé.
Le labium adhésif des Stenus est particulièrement efficace, et fait de ces staphylins des prédateurs très redoutables. Il peut se fixer tant sur des cuticules lisses que sur des cuticules aux microsculptures variées présentes dans un large éventail de proies potentielles (voir photo de cuticules de collemboles ci-dessus ou cliquer ici).
Le « harpon labial » est composé (photo ci-dessous) d'un prémentum distal allongé en forme de tige relié à la tête par une membrane conjonctive également étirée. Au repos, elle est invaginée dans la tête comme un doigt retourné à l’intérieur d'un gant. L'appareil de capture fonctionne telle une catapulte : avant la frappe, le labium est comprimé par la pression de l'hémolymphe, puis est soudainement relâché, et projeté vers l'avant du corps en 4 à 5 millisecondes.
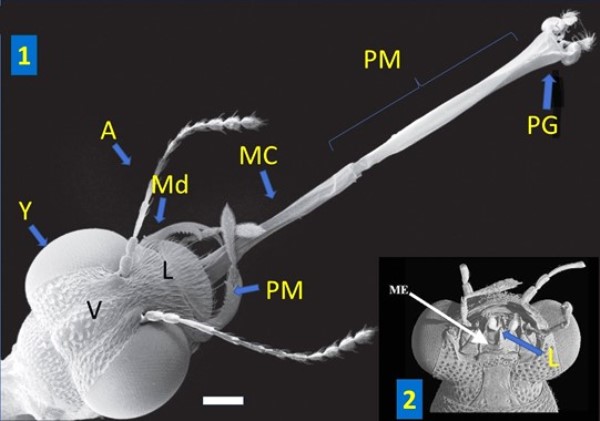 Photos au microscope électronique à balayage de têtes de Stenus sp.
Photos au microscope électronique à balayage de têtes de Stenus sp.
1. Stenus bimaculatus Gyllenhal, 1810 avec le labium dévaginé. Vue dorsale. A : antenne, Md : mandibule, PM : palpe maxillaire, L : labre, MC : membrane connective, ME : mentum ; PG : paraglosse, PM : prémentum, V : vertex, Y : yeux. Modifié d’après © Betz, 2016. Échelle : 200 µm.
2. Vue ventrale de la tête de Stenus sp. avec le labium (L) en position de repos. Modifié d’après © Żyła et al., 2017. Échelle : 200 µm.
À son extrémité, le prémentum (voir photo ci-dessous) possède deux paraglosses modifiées en coussinets adhésifs constitués par une multitude de trichomes ramifiés (longues soies creuses) qui en augmente la surface adhésive.
La forme de ces paraglosses (et donc la surface adhésive) a évolué en fonction des proies recherchées par les diverses espèces de Stenus. Ainsi, on trouve des coussinets ellipsoïdaux, ovales, longiformes, coniques…
La membrane de connexion et le prémentum sont parcourus par des faisceaux de canalicules longitudinaux qui transportent, vers les coussinets adhésifs, la sécrétion adhésive produite par des glandes sécrétrices situées dans la tête. Ces dernières sont constituées d’unités glandulaires distinctes, chacune composée de trois cellules. Deux de ces cellules sont des cellules sécrétrices actives, l’une produisant des sécrétions protéinées, l’autre des sécrétions lipoïdes. Conséquemment, on observe une sécrétion en deux phases sur les paraglosses. Les canalicules glandulaires qui vont des glandes aux paraglosses servent également de réservoir aux sécrétions avant leur évacuation juste avant l’attaque d’une proie.
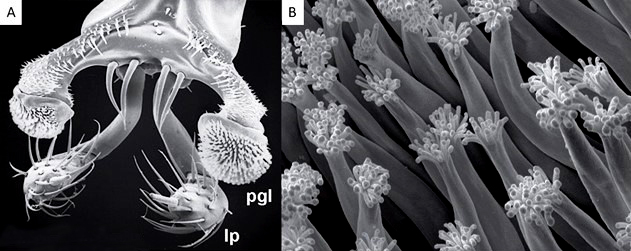 Photos au microscope électronique à balayage de l’extrémité du labium de Stenus sp.
Photos au microscope électronique à balayage de l’extrémité du labium de Stenus sp.
A. Stenus comma LeConte, 1863. Vue dorso-frontale de l’extrémité du labium dévaginé. Pgl : paraglosse et lp palpe labial. Échelle 100 µm. Modifié d’après © Betz, 2006.
B. Stenus bimaculatus Gyllenhal, 1810. Détail de l’extrémité des trichomes adhésifs. Échelle 2 µm. Modifié d’après © Koerner et al., 2016.
Les forces de Van der Waals1 de même que la tension de surface2 et la viscosité des sécrétions adhésives sont envisagées comme mécanismes possibles de l’adhésion nécessaire pour capturer les collemboles, par exemple.
Le gel collant est envahi par de très nombreuses de bactéries appartenant aux Actinomycétales (Arthrobacter, Microbacterium, Rhodococcus) et aux Pseudomonadales (Acinetobacter, Pseudomonas). Leur fonction reste encore à définir. Elles augmentent peut-être les propriétés adhésives du gel tapissant les coussinets.
La présence de résiline dans la paroi des trichomes les rend très flexibles et élastiques, de sorte qu'ils peuvent s'adapter étroitement à la forme et aux irrégularités de surface de la proie (voir article de ce site : microstructure de la cuticule des collemboles). Comme le « labium-harpon » est utilisé plusieurs centaines de fois au cours de la vie du coléoptère pour capturer des proies, la résiline assure la résistance des coussinets à l’usure, de façon similaire à la fonction de la résiline dans les plis des ailes des staphylins, repliées- au repos- de nombreuses fois sous les élytres.
Par rapport à la possibilité de capturer un insecte en le saisissant simplement avec les mandibules, la valeur adaptative du « harpon-labial » réside à la fois dans sa vitesse d’exécution et sa portée supérieures, ainsi que dans sa capacité à fixer la proie au moment du contact.
 Ainsi, même les Stenus ayant une activité et une réactivité limitées sont capables de capturer des invertébrés autrement insaisissables, d'une manière étonnamment rapide et efficace.
Ainsi, même les Stenus ayant une activité et une réactivité limitées sont capables de capturer des invertébrés autrement insaisissables, d'une manière étonnamment rapide et efficace.
Néanmoins, la technique de capture des proies par les mandibules a également évolué chez certains Stenus très agiles et réactifs, vivant sur le sol dans des habitats ouverts : les plus grandes proies- aux mouvements de fuite puissants- sont insaisissables avec le « labium-harpon », les forces d’adhésion des coussinets n’étant pas suffisantes pour les maintenir fermement, elles sont alors attrapées et immobilisées avec les mandibules. Cette immobilisation est renforcée par la grande dent et les denticules parsemant le côté interne des fines mandibules.
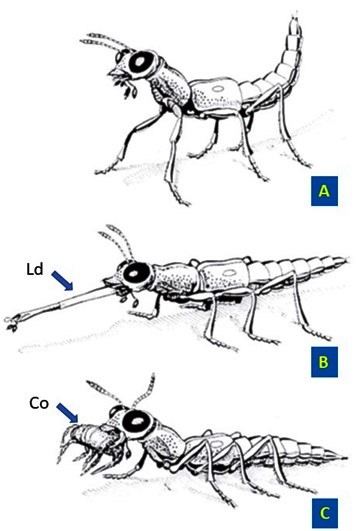
Les dessins ci-contre illustrent les trois phases d’une chasse au « harpon » de Stenus comma LeConte, 1863.
(Taille de l’insecte : 5,5 mm. Modifié d’après © Betz, 2006).
A. Le Stenus a repéré visuellement sa proie et s’est positionné à une distance lui permettant de l’atteindre.
B. En exerçant une vive pression sur son hémolymphe, il dévagine son labium (Ld) qui se propulse à très grande vitesse vers sa proie.
C. Une fois sa proie (Co) saisie grâce aux trichomes adhésifs qui recouvrent ses paraglosses, le labium se rétracte et ramène la proie vers les mandibules.
Désormais, nous connaissons mieux le Stenus, et pouvons revenir plus en détail sur ses stratégies d’attaques dirigées en l’occurrence contre les trois espèces de collemboles mentionnés plus haut.
- 1 Correspondent à une interaction électrique d'intensité faible ayant lieu à courtes distances entre atomes et/ou molécules.
- 2 Peut être définie brièvement comme étant la force qui existe au niveau d'une interface entre deux milieux.
5) Stratégies : Attaque-Défense
Un collembole détecte l’approche d’un prédateur par plusieurs voies sensorielles tels les yeux ou grâce à des percepteurs mécano-sensoriels et/ou chimiques (voir : Soies et sensilles et PAO )
Généralement, les grands collemboles évitent le contact direct en fuyant vers l’avant, sur une distance plutôt constante. Ce comportement de fuite opère déjà une sélection chez les prédateurs et écarte les espèces de Stenus les plus maladroites ou les moins véloces.
Comment les Stenus ont-ils, durant leur coévolution avec les collemboles, optimisé leur chasse ?
Le labium extensible, utilisé tel un harpon, autorise une distance prédateur/proie plus grande qui éveillera moins la vigilance de la proie. Les chercheurs ont également observé que lors de leurs attaques, les Stenus « harponneurs » se précipitent vers leur proie simultanément au déploiement de leur labium, ce mouvement réduit la probabilité de fuite du collembole et augmente la probabilité de la capture.
La vitesse de course mesurée sur des échantillonnages de « grands » collemboles (taille moy. stade adulte : 2.5 à 3.0 mm) est comprise entre 1.77 et 2.78 mm/s et elle se situe entre 0.90 et 1.18 mm/s pour les petits (taille moy. stade adulte ≤ 2.0 mm) Ces vitesses expliquent notamment pourquoi les grands collemboles sont plus difficiles à capturer par les Stenus. Comme déjà évoqué, la masse corporelle du collembole constitue aussi un facteur important à corréler avec la capacité adhésive du labium du prédateur. Plus la proie sera lourde, plus importante devra être l’adhésivité de l’extrémité du labium.
Enfin, certains Stenus (tels S. comma LeConte, 1863 - S. fossulatus Erichson, 1840 et S. canaliculatus Gyllenhal, 1827) qui chassent à terrain découvert, ont affiné leurs techniques de prédation au point d’être capables de saisir de gros collemboles à l’aide de leurs mandibules avec un taux de réussite important (25 à 40 %). Tandis qu’a contrario, le taux de réussite est de seulement 2 % pour les attaques de S. fossulatus utilisant son labium pour atteindre un « gros » collembole.
Sans entrer dans le détail des différentes études conduites sur le sujet, on peut avancer que, de manière générale, les Stenus chassent plutôt les petits collemboles en utilisant leur labium, alors qu’ils ont plutôt tendance à employer leurs mandibules pour capturer les gros Collemboles.
6) Etude comportementale des collemboles :
Les données et comptages de déplacements de trois espèces de collemboles sont résumées dans le tableau ci-dessous. Elles ont été mesurées sur 5 individus de chaque espèce. Les spécimens étudiés ont été déposés dans une cuvette en verre et filmés durant 11 minutes. Comme l’indiquent ces résultats, les comportements de ces taxons ne sont pas homogènes et peuvent même présenter de fortes variations.
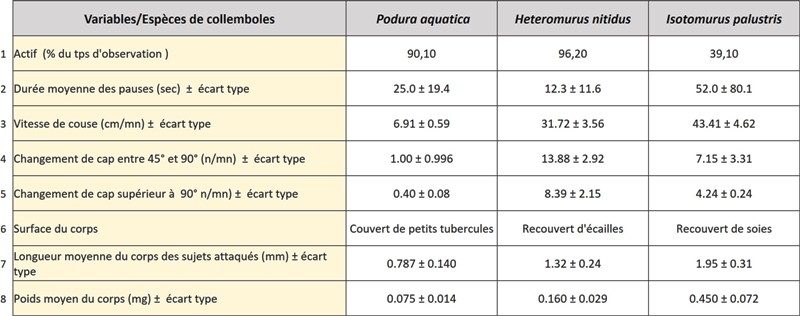
Analyse du tableau :
- Ligne 1 : pourcentage moyen de collemboles actifs durant le temps d’observation. P. aquatica et H. nitidus se détachent nettement et se montrent plus de deux fois plus actifs qu’I. palustris. Noter que l’un d’entre nous (Ph. G.) a observé que H. nitidus, vivant sur les couches superficielles du sol et sur des terrains fermes, se déplace en faisant peu de pauses et en furetant en tous sens. Les P. aquatica, en revanche, se meuvent assez lentement et, comme ils évoluent souvent dans des zones aquatiques, ils s’agitent beaucoup, sans que leurs déplacements se montrent très efficaces, et ce, en raison des griffes pointues de l’extrémité de leurs pattes, peu adaptées au déplacement sur la surface l’eau (la portance étant assurée par la force de tension superficielle de l’eau).
- Ligne 2 : durée moyenne des pauses qu’effectuent les 3 espèces de collemboles entre leurs périodes actives. I. palustris, avec ses pauses de deux à quatre fois plus longues que les deux autres espèces, serait une cible plus aisée pour un prédateur chassant à l’affût comme un Stenus.
- Ligne 3 : vitesse de fuite par la course en cm par minute. I. palustris est nettement plus rapide que P. aquatica et, dans une moindre mesure, que H. nitidus. Sur base de ce paramètre, P. aquatica a plus de risque de se faire « harponner » par un Stenus.
- Lignes 4 et 5 : nombre de changements de trajectoires par minute avec un angle compris respectivement entre 45° et 90° et supérieur à 90°. Ces lignes indiquent que P. aquatica se déplace de manière quasi rectiligne, alors que H. nitidus change de cap en moyenne toute les 3 secondes et I. palustris toutes les 5 à 6 secondes, ce qui confirme les observations de l’un d’entre nous (Ph. G.). Dès lors, sur base de ces trajectoires, P. aquatica serait une proie plus facile pour un Stenus.
- Ligne 6 : L’adhésion des coussinets de l’extrémité du labium (voir texte et photos ci-dessus pour plus détails) sera d’autant plus importante et forte sur une surface accidentée plutôt que sur une surface plus lisse, comme chez P. aquatica (voir photos ci-dessous).
- Lignes 7 et 8: longueur et poids moyens des collemboles. Plus l’espèce sera grande et lourde (I. palustris), plus elle aura de chance d’échapper au « harpon » des Stenus.
Toutes ces données assez disparates soulignent que chacune des trois espèces de collemboles ne dispose pas des mêmes capacités défensives. A priori, face à un prédateur comme un Stenus, P. aquatica semblerait relativement désavantagé par rapport à sa vitesse de déplacement lente, à sa très faible capacité à changer de direction, à sa taille et son poids moindres, mais également à son écologie (il évolue dans des habitats qu’affectionne particulièrement les Stenus).
 Podura aquatica sur l’eau, en bordure d’un étang à 1800 m d’altitude © Ph. Garcelon.
Podura aquatica sur l’eau, en bordure d’un étang à 1800 m d’altitude © Ph. Garcelon.
7) Analyse des attaques sur les collemboles.
Préalable : L’observation et le comptage des attaques, nécessitent la mise en place d’un matériel de prise de vue et d’éclairage élaboré que nous ne détaillerons pas ici. Il faut cependant savoir que pour filmer ces mouvements d’attaque très rapides (mesurables en millisecondes), les chercheurs ont utilisé des caméras capables d’enregistrer des images à des cadences de 1000 à 1050 images/seconde.
Pour effectuer leurs observations, les collemboles ont été placés dans des situations identiques face à leurs prédateurs. Les Stenus ont été prélevés dans leur habitat naturel, en bordure d’un étang de sablière puis conservés dans des boites, sur un substrat de plâtre de Paris humidifié, maintenu à une température constante de 20°C. Ils ont été volontairement affamés durant quatre à cinq jours. Les collemboles ont été capturés dans l’habitat du Stenus ou proviennent de cultures effectuées en laboratoire. Conservés eux aussi sur du plâtre humide mais nourris avec des flocons de soja.
 Les chercheurs ont, dans un premier temps, essayé d’évaluer la distance à laquelle le Stenus repérait sa proie. Pour cela, ils ont choisi de confronter le Stenus avec Heteromurus nitudus (1.5 mm) et Podura aquatica (0.8 mm) en raison de leur différence de taille significative. Ils ont utilisé pour leur expérimentation des boites de 6 cm de diamètre dans lesquelles ils ont, à chaque fois, confronté un Stenus à trois collemboles de même espèce. Ils ont utilisé 18 Stenus pour mener à bien cette expérience, au terme de laquelle ils ont pu évaluer 160 évènements par espèce de collembole.
Les chercheurs ont, dans un premier temps, essayé d’évaluer la distance à laquelle le Stenus repérait sa proie. Pour cela, ils ont choisi de confronter le Stenus avec Heteromurus nitudus (1.5 mm) et Podura aquatica (0.8 mm) en raison de leur différence de taille significative. Ils ont utilisé pour leur expérimentation des boites de 6 cm de diamètre dans lesquelles ils ont, à chaque fois, confronté un Stenus à trois collemboles de même espèce. Ils ont utilisé 18 Stenus pour mener à bien cette expérience, au terme de laquelle ils ont pu évaluer 160 évènements par espèce de collembole.
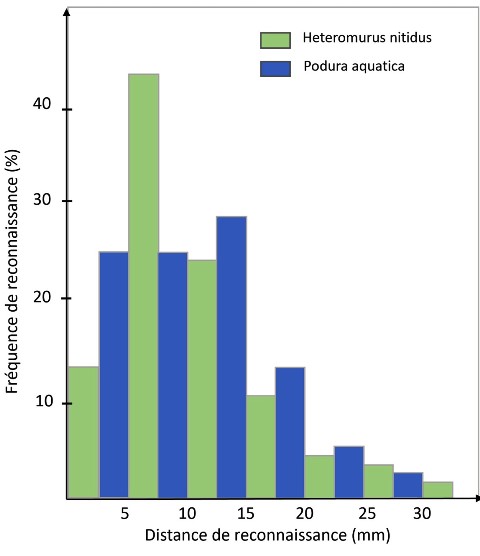
L'histogramme ci-contre résume les distributions de la fréquence de reconnaissance par rapport à la distance entre la proie et son prédateur.
La distance de reconnaissance étant définie comme celle entre l’extrémité de la tête du staphylin et la partie la plus proche de sa proie.
Le tableau ci-dessous indique quant à lui que la fréquence de reconnaissance atteint son maximum (+ de 40 %) pour Heteromurus nitidus entre 6 et 10 mm. Au-delà de 15 mm, elle chute à moins de 10%. Pour Podura aquatica, les amplitudes en fonction de la distance sont moins accentuées et la plage plus élargie (comprise entre 5 et 20 mm, avec un taux de reconnaissance moyen légèrement supérieur à 25 %).
De manière plus générale on remarque qu’au-delà de 15 mm le taux de reconnaissance est voisin de 10 % et chute autour de 5 % au-delà de 20mm pour descendre à moins de 1% pour des distances supérieures à 30 mm.
8) Discussion :
Les situations reproduites par les chercheurs ne sont pas tout à fait identiques à celles rencontrées par les populations étudiées au sein de leurs habitats respectifs. En effet, la nature des zones dans lesquelles elles évoluent est difficile à traduire sous forme de chiffres car trop de variables sont à prendre en ligne de compte. Les éléments chiffrés donnés ici représentent cependant la meilleure approche possible en laboratoire. Idéalement il faudrait effectuer les mesures « in situ » ce qui en pratique est excessivement difficile à réaliser.
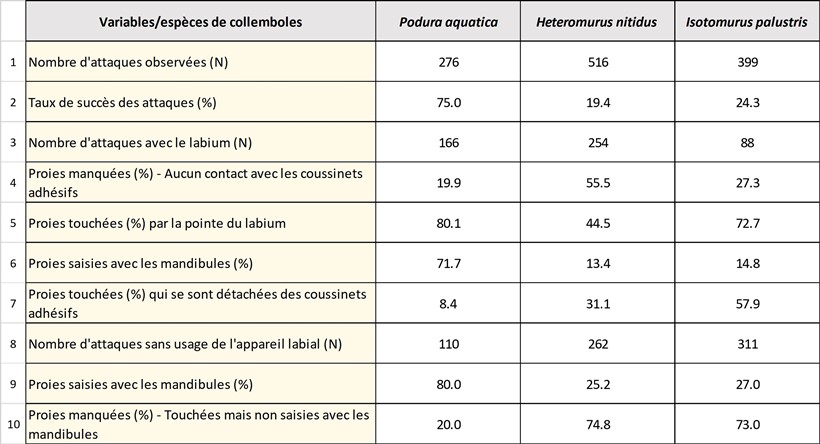
Le tableau d’analyse des attaques du Stenus signale un taux de réussite plus faible (ligne 2) avec les plus grands collemboles. En effet, à la ligne 8, on remarque que les grands collemboles (H. nitudus 1.32 mm et I. palustris 1.95 mm), couverts d'écailles (H. nitidus) ou de soies (I. palustris) présentent une plus forte propension à se détacher de l’extrémité du labium (ligne 7). On notera également que le P. aquatica, dont la trajectoire est la plus rectiligne, et présente la vitesse de fuite (6.9 cm/mn) la plus faible (H. nitidus : 31.7 cm/mn et I. palustris : 43.4 cm/mn) est l’espèce la plus exposée (ligne 10).
Si enfin, on calcule le pourcentage d’attaques réalisées avec les mandibules (sans usage du labium) par rapport au total des attaques, on trouve 39.8% pour P. aquatica, 58.8 % pour H. nitidus et 77.9 % pour I. palustris.
Ce qui tendrait à montrer que les Stenus sont capables d’intégrer certaines variables relatives à leurs proies (taille, vitesse de fuite, changement de direction…) pour effectuer leurs choix stratégiques et adapter au mieux leur mode de chasse.
Bibliographie :
- Bauer TH. & M. Pfeiffer (1991). 'Shooting' springtails with a sticky rod: the flexible hunting behaviour of Stenus comma (Coleoptera; Staphylinidae) and the counter-strategies of its prey. Anim. Behav., 41 : 819-828.
- Betz O. (1996). Function and evolution of the adhesion-capture apparatus of Stenus species (Coleoptera, Staphylinidae). Zoomorphology 116:15–34.
- Betz O (1998). Comparative studies on the predatory behaviour of Stenus spp. (Coleoptera: Staphylinidae): the significance of its specialized labial apparatus J. Zool., Lond. 244, 527-544.
- Betz, O (2006). Der Anpassungswert morphologischer Strukturen: Integration von Form, Funktion und Ökologie am Beispiel der Kurzflügelkäfergattung Stenus (Coleoptera, Staphylinidae). Entomologie heute 18 : 3-26.
- Betz O., Koerner L. & L. Dettner (2018). The Biology of Steninae. In: Betz O., Irmler U. & J. Klimaszewski J. (eds) : Biology of Rove Beetles (Staphylinidae). Springer, Cham. 229-283. https://doi.org/10.1007/978-3-319-70257-5_11.
- Cai C., Clarke D.J. Yin Z., Fu Y. & D. Huang (2019). A specialized prey-capture apparatus in mid-Cretaceous rove beetles. Current Biology, Vol. 29 (4) : R116 - R117. https://doi.org/10.1016/j.cub.2019.01.002
- Koerner L., Stanislav N., Gorbb S.N. & O. Betz (2011). Functional morphology and adhesive performance of the stick-capture apparatus of the rove beetles Stenus spp. (Coleoptera, Staphylinidae). Zoology Vol. (115, 2) : 117-127. https://doi.org/10.1016/j.zool.2011.09.006.
- Koerner L., Gorb S. & O Betz (2012). Adhesive performance of the stick-capture apparatus of rove beetles of the genus Stenus (Coleoptera, Staphylinidae) toward various surfaces. Journal of Insect Physiology, vol. 58 (1) : 155-163. https://doi.org/10.1016/j.jinsphys.2011.11.001.
- Koerner L. , Laumann M., Betz O. & M. Heethoff (2013). Loss of the sticky harpoon – COI sequences indicate paraphyly of Stenus with respect to Dianous (Staphylinidae, Steninae), Zoologischer Anzeiger - A Journal of Comparative Zoology, Vol. 252 (3) : 337-347. https://doi.org/10.1016/j.jcz.2012.09.002.
- Koerner L., Braun V. & O. Betz (2016): The labial adhesive pads of rove beetles of the genus Stenus (Coleoptera: Staphylinidae) as carriers of bacteria. Entomologia Generalis, 36 (1) : 33-41. https://doi.org/10.1127/entomologia/2016/0308.
- Koerner L., Garamszegi L.Z. , Heethoff M. & O. Betz (2017). Divergent morphologies of adhesive predatory mouthparts of Stenus species (Coleoptera: Staphylinidae) explain differences in adhesive performance and resulting prey-capture success. Zoological Journal of the Linnean Society, 181, 500–518.
- Kölsch G. (2000). The ultrastructure of glands and the production and function of the secretion in the adhesive capture apparatus of Stenus species (Coleoptera: Staphylinidae). Can. J. Zool. 78: 465–475.
- Żyła D., Yamamoto S., Schwenninger, W. K. & A. Solodovnikov (2017). Cretaceous origin of the unique prey-capture apparatus in mega-diverse genus: stem lineage of Steninae rove beetles discovered in Burmese amber. Sci Rep 7, 45904 (2017). https://doi.org/10.1038/srep45904.
